La termodinámica es la parte de la física que estudia la relación existente entre el calor y el trabajo
2. Termodinámica. Conceptos y magnitudes
Fenómeno "Rubber Band Heat Engine", demostración de como el calor puede producir un trabajo, o como podemos construir un motor con calor.
En primer lugar es necesario definir una serie de coneptos que serán utilizados a lo largo de este y los próximos temas:
Importante
Sistema: Porción de universo sometida a estudio termodinámico.
Entorno: Porción del universo que no es el sistema.
Calor, temperatura, energía interna
El calor es la energía que cede o absorbe un cuerpo cuando está en contacto con otro.
La caloría es la cantidad de calor necesaria para producir un incremento de temperatura de 1 °C en una muestra de agua con una masa de 1 g desde 14,5 °C hasta 15,5 °C. Se cumple que 1 cal = 4,1855 J.
La energía interna (U) es la energía total que poseen los cuerpos debido al incesante movimiento de las partículas que los componen. En los gases ideales, no hay interacciones entre las partículas que lo componen, por lo tanto la energía interna depende exclusivamente de la temperatura del sistema.
La temperatura hace referencia a la velocidad con que se mueven las partículas que forman un cuerpo, es decir mide la energía interna de un cuerpo. Una definición más técnica de la temperatura sería: "Medida macroscópica promedio de la energía cinética que poseen las partículas del sistema".
La energía interna de un cuerpo aumenta cuando aumenta su temperatura. El calor se transmite desde los cuerpos que se encuentran a mayor temperatura hacia los cuerpos con menor temperatura.
Sistemas termodinámicos
 |
| Imagen 3. Recurso propio. |
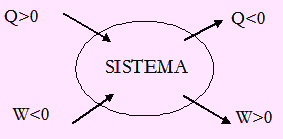
Sistema: Porción de universo sometida a estudio termodinámico.
Entorno: Porción del universo que no es el sistema.
Un sistema sólo puede intercambiar energía con su entorno de dos formas: trabajo o calor.
Los sistemas termodinámicos pueden ser:
- Sistemas abiertos: Se permite el intercambio de materia y energía con el ambiente.
- Sistemas cerrados: Solo es posible el intercambio de energía con el exterior.
- Sistemas aislados: No se permite el intercambio de materia ni energía con el exterior.
Para diferenciar energía que entra o sale al sistema es necesario establecer un convenio de signos, a lo largo de esta unidad se seguirá el siguiente convenio:
- Trabajo positivo: Trabajo hecho por el sistema, comunica energía al entorno.
- Trabajo negativo: Trabajo hecho sobre el sistema, toma energía del entorno.
- Calor positivo: Calor comunicado al sistema, toma energía del entorno.
- Calor negativo: Calor comunicado por el sistema, se aporta energía al entorno.
Realizamos algunas consideraciones:
- Por transformación termodinámica se entiende cualquier proceso en el que un sistema pasa de un estado inicial a un estado final en el que alguna de las propiedades que sirven para describirlo ha variado.
- Un aspecto muy importante a tener en cuenta es que hay propiedades cuyo valor solamente depende del estado en que se encuentra el sistema. Estas propiedades reciben el nombre de funciones de estado.
- La energía interna es una función de estado. También lo son la presión, la temperatura y el volumen. Sin embargo el calor y el trabajo no lo son. Esto es así por dos motivos: en primer lugar calor y trabajo no son propiedades del sistema sino que son formas de energía en tránsito. En segundo lugar su valor en una transformación dependerá del camino seguido, tal y como se vio en el tema anterior cuando se presento el concepto Trabajo.
- Las funciones de estado de un sistema en equilibrio estarán relacionadas por medio de las ecuaciones de estado. En el caso de los gases ideales, esta ecuación es la ecuación de estado de los gases ideales:
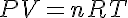 . Donde P es la presión del sistema, V el volumen, n el número de moles gaseosos contenidos en el sistema, T la temperatura y R la constante de los gases ideales, cuyo valor en unidades SI es 8.314 J/mol.K
. Donde P es la presión del sistema, V el volumen, n el número de moles gaseosos contenidos en el sistema, T la temperatura y R la constante de los gases ideales, cuyo valor en unidades SI es 8.314 J/mol.K - Como veremos más adelante las máquinas térmicas funcionan repitiendo ciclos termodinámicos. Un ciclo termodinámico es todo proceso en el que un sistema parte de un estado inicial, sufre una serie de transformaciones termodinámicas tras las cuales llega a un estado final igual al inicial. Según esto y dado que la energía interna es una función de estado, es decir, depende de los valores iniciales y finales, en todo ciclo termodinámico se cumplirán:
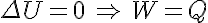 . Es decir la energía interna no variará y el calor neto comunicado al sistema será igual al trabajo realizado por el mismo.
. Es decir la energía interna no variará y el calor neto comunicado al sistema será igual al trabajo realizado por el mismo.
Resumimos:
Son funciones de estado: presión, temperatura, volumen, energía interna. Sus valores dependen de los estados inicial y final de un sistema.
No son funciones de estado: calor y trabajo. Su valor depende de la trayectoria seguida por el sistema entre los estados inicial y final.